Da Apple efter sigende går på markedet med iWatch, mødes de også med FDA, hvilket understøtter rygter om iWatchs avancerede medicinske potentiale.
Apples iWatch, som i øjeblikket er genstand for industrirygter og forbrugernes nysgerrighed, er klar til at transformere sundhedsindustrien. Pundits har spekuleret i, at iWatch vil være i stand til at levere en bred vifte af medicinske data til alle fra løbere interesseret i toppræstationer til skadestuepersonale, der har brug for hurtig statistik at behandle patienter. Fra puls- og hydreringsstatistikker til glukoseniveauer for diabetikere, lover iWatch at innovere branchen.
Apple ser ud til at forstå udmærket, at deres største hindring for at komme på markedet med iWatchs medicinske teknologi kunne være den amerikanske fødevare- og lægemiddeladministration (FDA). FDA definerer mobile apps/enheder som "softwareprogrammer, der kører på smartphones og andre mobile kommunikationsenheder. De kan også være tilbehør, der kan tilsluttes en smartphone eller andre mobile kommunikationsenheder, eller en kombination af tilbehør og software." (7) Fordi iWatchs medicinske teknologi kan potentielt udgøre en risiko for de mennesker, der kan bruge den. FDA skal muligvis gennemgå eventuelle medicinske iWatch-applikationer før lancering.
Indhold
- At dyrke relationer
-
Det ventende spil
- Relaterede indlæg:
At dyrke relationer
Det er sandsynligt, at Apple har haft øje på denne forhindring i et stykke tid. Faktisk har Apples ledere mødtes med FDA-embedsmænd siden kort efter lanceringen af den første iPad i april 2010.
Apple-chefer vidste, at der var et enormt potentiale for iPad i den medicinske industri. Fra det øjeblik, iPad blev lanceret, omfavnede læger iPad'en, og i juli 2010 befolkede mere end 2.000 medicinske apps Apples App Store. (3)
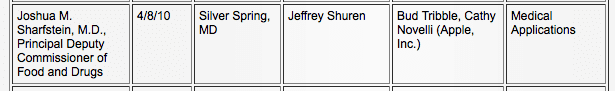
Da potentialet for iPad'en som en spiller i den medicinske industri voksede, dyrkede Apple et forhold til FDA. Ifølge FDA's offentlige optegnelser har Apple og FDA mødtes tre gange, først den 8. april 2010, at tale om "medicinske applikationer" (5) og igen den 11. juni 2010 om emnet "medicinsk udstyr". (6)

FDA's opgave er at balancere offentlig sikkerhed med offentlighedens interesse. Efter disse to møder, i juli 2011, udgav FDA sin første iteration af definitioner og retningslinjer for mobile medicinske applikationer. (8) I september 2011 lancerede Apple en sektion kaldet "Apps til sundhedsprofessionelle" i sin App Store (4) med sundheds-tema apps til reference og uddannelse samt mere avancerede apps, herunder elektroniske lægejournaler (EMR), patientovervågning og billeddannelse.
Det ventende spil
Apples ledere var tilbage hos FDA i december 2013 for at diskutere "mobile medicinske applikationer", en klar indikation at Apple har bevæget sig ind på sundhedsovervågningsteknologiområdet nok til at vide, at de skal tale med FDA kl længde.

FDA har forfinet sine definitioner og politikker omkring medicinske applikationer og udstyr. "Nogle mobilapps indebærer minimale risici for forbrugere eller patienter, men andre kan bære betydelige risici, hvis de ikke fungerer korrekt," udtalte en nylig FDA-pressemeddelelse og tilføjede: "FDA's skræddersyede politik beskytter patienter, mens den opmuntrer innovation." (2)
Pressemeddelelsen fortsatte:
FDA fokuserer sit tilsyn på mobile medicinske apps, der:
- er beregnet til at blive brugt som tilbehør til et reguleret medicinsk udstyr – for eksempel en applikation, der gør det muligt for en sundhedsperson at tage en specifik diagnose ved at se et medicinsk billede fra et billedarkiverings- og kommunikationssystem (PACS) på en smartphone eller en mobil tablet; eller
- transformere en mobil platform til et reguleret medicinsk udstyr – for eksempel en applikation, der forvandler en smartphone til en elektrokardiografi (EKG) maskine til at opdage unormale hjerterytmer eller afgøre, om en patient oplever et hjerteanfald." (2)
Noget af den funktionalitet, som iWatch siges at stræbe efter, falder bestemt under FDA's tilsyn retningslinjer for medicinske mobilenheder og apps, der udsætter Apple for samme FDA-kontrol som andre producenter.
Hvordan vil FDA-bestemmelser, gennemgang, godkendelser og processer påvirke udgivelsen af en medicinsk version af Apples iWatch? Tag tilfældet med Smart Body Analyzer, et produkt fra Withings, der måler vægt, kropsfedtprocent og puls og synkroniserer med smartphones og iPads. Withings ventede i næsten tre år på at få FDA-godkendelse til at lancere.(1) Apples mere sofistikerede funktionalitet kan betyde længere godkendelsestid af FDA, men måske ved at mødes med FDA i udviklingsstadierne, vil Apple have købt noget tid, som det går til marked.

Sudz (SK) er besat af teknologi siden den tidlige ankomst af A/UX til Apple, og er ansvarlig for den redaktionelle ledelse af AppleToolBox. Han er baseret i Los Angeles, CA.
Sudz har specialiseret sig i at dække alt hvad angår macOS, efter at have gennemgået snesevis af OS X- og macOS-udviklinger gennem årene.
I et tidligere liv arbejdede Sudz med at hjælpe Fortune 100-virksomheder med deres ønsker om teknologi og forretningstransformation.